

FDA是美国食品药品监督管理局(U.S.Food&Drug Administration)的简称,是美国食品与药品管理的最高执法机关,世界各国都会在一定程度上参考或依据FDA的相关法规来评估本国食药类产品的安全。FDA召回则是一种对于不合格产品采取的撤回弥补行为,被召回的产品大致分为以下几类:食品(包括个人护理产品)、药品、生物制剂、设备、兽药。
今天小编将对2013-2019年FDA药品召回事件中,涉及微生物污染的召回事件进行一个简单的回顾性分析。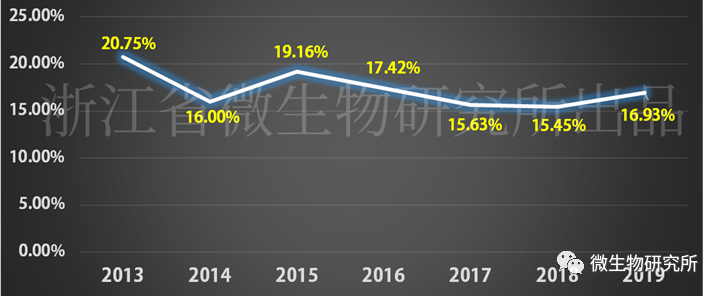
微生物相关的召回事件占总事件的比例变化
2013-2019年药物召回共有2327起,其中共有401起召回涉及微生物,占药品召回总数的17.23%。涉及微生物的召回药品中,无菌产品284起,非无菌产品117起。其中大部分的召回原因是缺乏无菌保证,有267起。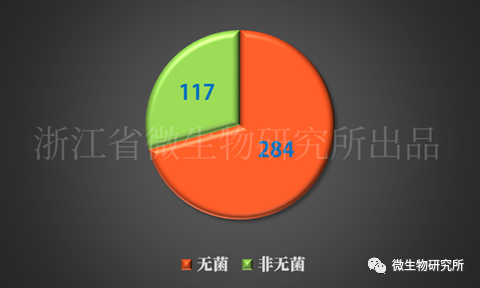
在微生物相关的召回事件中的无菌产品和非无菌产品的召回次数
在非无菌产品是指可以接受微生物存在的产品,但是产品中的微生物数量不能超过一定限度(微生物数量超限表明产品的生产环境或生产过程可能不受控)且不得检出法规明确规定的控制菌以及“不可接受微生物”。在117起非无菌产品的召回中,55起召回并未注明具体的污染微生物物种;在注明污染物种的召回中,真菌(酵母/霉菌)和细菌污染分别占19%和32%。而细菌污染中占比最大的污染菌为Burkholderia cepacia complex(洋葱伯克霍尔德复合体),比例达到30.67%。其他曾在非无菌产品召回中出现过的细菌有:Escherichia. coli(大肠埃希氏菌)、Pseudomonas sp.(假单胞菌属)、Sphingomonas paucimobilis(少动鞘氨醇单胞菌)、Serratia liquefaciens(液化沙雷氏菌)、Staphylococcus warneri(沃氏葡萄球菌)、Staphylococcus aureus(金黄色葡萄球菌)、Klebsiella pneumoniae(肺炎克雷伯氏菌)、Bacillus circulans(环状芽孢杆菌)、Variovorax paradoxus(争论贪噬菌)、Pseudomonas aeruginosa(铜绿假单胞菌)等。
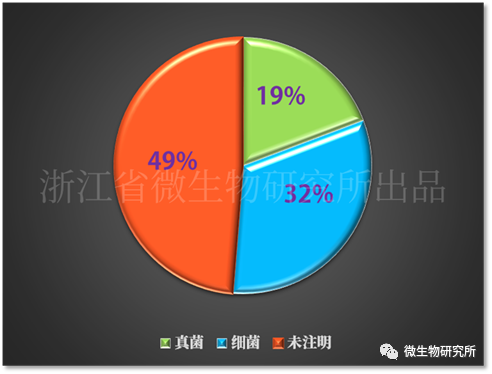
非无菌产品微生物相关召回中污染菌的类型
在《中国药典》2015版第四部和美国药典《USP》中,都有非无菌药品在微生物检查方面的相关规定,例如在“非无菌药品的微生物限度检查”中,明确根据给药途径规定了一些控制菌,其中包括大肠埃希菌、沙门氏菌、金黄色葡萄球菌、铜绿假单胞菌、白色念珠菌等;另外,对于药品中的需氧菌总数、霉菌和酵母菌总数也有相关的规定。在本次统计的FDA召回的非无菌产品中,Burkholderia cepacia complex(洋葱伯克霍尔德复合体)污染是涉及召回次数最多的微生物,在2004~2011年的非无菌产品汇总中,Burkholderia cepacia complex(洋葱伯克霍尔德复合体)也是召回产品中污染占比最高的菌。起初,Burkholderia cepacia complex(洋葱伯克霍尔德复合体)并未被列入控制菌范围内,它对药品的潜在威胁性是在2018年9月底举行的PDA/FDA会议中被提出的。目前,在2019年12月1日生效的《美国药典》中,已经将Burkholderia cepacia complex(洋葱伯克霍尔德复合体)纳入了控制菌检查项目。
我们不能因为某些人吃海鲜过敏而禁止所有人食用海鲜,同样的,不能因为药品中存在微生物对于某些人群有害而禁止所有人使用,因此对于是否判定为“不可接受微生物”对于不同的药品生产厂家可能也需要有更为详细的考量因素,例如:药品的给药途径、药品的特性(是否促进微生物生长或者是否有足够的抑制微生物生长能力)、药品的使用方法、用药人群(如新生儿、婴幼儿及体弱者,风险可能不同)、患者使用免疫抑制剂和甾体类固醇激素等药品;存在疾病、伤残和器官损伤等。在21 CFR 211.84(d)(6) ,21 CFR 211.113(a),21 CFR 211.165(b)提供了对“不可接受生物”的一些指导原则。不过,这些指导原则并未对”不可接受微生物“做出定义。监管机构也不提供“不可接受微生物“的列表,而是希望生产厂商通过分析来决定自己产品里的“不可接受微生物“,并进行相应的质量控制。在cGMP(动态药品生产管理规范)中,对“不可接受微生物”也没有进行详细的规定,但是其一般具有以下几个属性:首先,这个概念是针对非无菌产品的。对无菌产品而言,所有的微生物都不可接受;
其次,不可接受微生物是产品特异的。可在特定的产品中增殖,对该药品的化学、物理、功能和治疗属性产生不利影响的微生物;
另外,在产品中有足够的数量并因具有致病性而在给药时可导致患者感染的微生物,也被认为是不可接受的。
在《中国药典》2015版第四部提到:对于原料、辅料及某些特定的制剂,根据辅料及其制剂的特性和用、制剂的生产工艺因素,可能还需检查其他有潜在危害的微生物,可见药典中也没有详细列出哪些是“不可接受微生物”。以Burkholderia cepacia(洋葱伯克霍尔德氏菌)为例,该菌是一种严重的机会性人类病原体,参与囊性纤维化患者的感染,且对多种抗生素有耐药性,且在一些消毒剂、防腐剂中也能找到该菌的存在,对于免疫力较强的健康人可能不致病,但是对于新生儿、晚期老年和囊性纤维化患者(包括其他患者)尤其危险,如果药物是用于这类人群则不应有Burkholderia cepacia(洋葱伯克霍尔德氏菌)存在,另外也不应存在于用于鼻腔通道或者肺部的药物中。那么除了Burkholderia cepacia complex(洋葱伯克霍尔德复合体),是否可能存在其他“不可接受微生物”?还有哪些条件致病菌也可以被列为特定类型药品的“不可接受微生物”?与其被动的等待微生物污染事件爆发后的总结归纳,我们更应该做的是防范于未然。通过对生产环境和产品进行一定水平的微生物监测,结合临床等其他信息,尽可能的去识别和发现那些可能对药品质量或者人体健康存在重要影响的微生物,并将它们纳入“不可接受微生物”控制列表,从源头上扼制可能发生的危害,以避免患者的生命健康受到威胁,也避免对医药企业自身造成经济损失。